Prevención de la enfermedad por CMV en receptores de trasplante de riñón D+/R- de alto riesgo1,2
Diseño del estudio: ensayo clínico fase 3, multicéntrico, doble ciego, controlado por comparador activo, de no inferioridad en pacientes adultos con trasplante de riñón de alto riesgo (D+/R-) que recibieron PREVYMIS junto con aciclovir una vez al día versus valganciclovir junto con un placebo frente a aciclovir (N=589). La profilaxis se inició desde el día 0 al 7 y se continuó hasta la semana 28 (~200 días) post-trasplante. El criterio de valoración principal de eficacia fue la incidencia de enfermedad por CMV (enfermedad por CMV de órganos terminales o síndrome CMV, confirmado por un comité de adjudicación independiente) hasta la semana 52 después del trasplante.3
PREVYMIS fue no inferior a valganciclovir en la prevención de la enfermedad por CMV postrasplante (criterio de valoración principal)3
Porcentaje de pacientes con enfermedad por CMV hasta la semana 52 después del trasplante (enfoque de falla observada [OF])3

aCasos de enfermedad por CMV confirmados por un comité de adjudicación independiente.3
bBasado en un margen de no inferioridad del 10 %, PREVYMIS es no inferior a valganciclovir.3
Enfoque para el manejo de valores perdidos: enfoque OF. Con el enfoque OF, los sujetos que suspendieron prematuramente el tratamiento en estudio por cualquier motivo no se consideraron fracasos.3
Enfermedad por CMV hasta la semana 28 (~200 días) después del trasplante3
Pacientes con enfermedad por CMV hasta la semana 28 (~200 días) después del trasplante3

cCasos de enfermedad por CMV confirmados por un comité de adjudicación independiente.3
dResultado secundario de eficacia.3
Análisis post hoc del estudio de fase 3
En este estudio de fase 3, doble ciego y controlado con placebo, los pacientes fueron aleatorizados para recibir PREVYMIS 480 mg por vía oral una vez al día 6 y aciclovir 400 mg por vía oral dos veces al día (dosis de aciclovir ajustada para la DepCreat) o valganciclovir 900 mg por vía oral una vez al día (dosis ajustada para DepCreat) con placebo equivalente a aciclovir dos veces al día.3,4
Limitaciones del análisis post-hoc4
- Análisis post hoc y de subgrupos.4
- El análisis se realizó hasta la semana 28 después del trasplante de riñón; sin embargo, el criterio de valoración principal del estudio se evaluó hasta la semana 52.4
- El análisis no tuvo la potencia necesaria para mostrar diferencias entre los brazos de profilaxis.
- El estudio excluyó a pacientes con DepCreat ≤10 ml/min.5
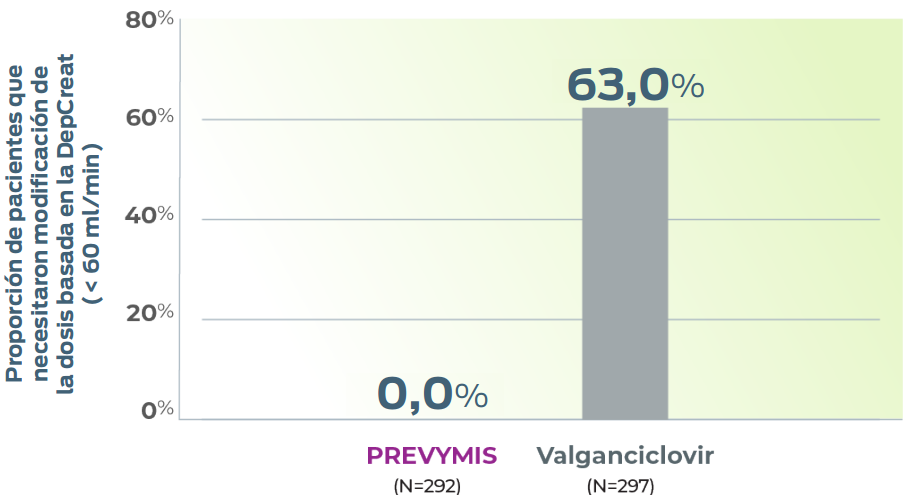
Modificaciones de dosis debido a la DepCreat (<60 ml/min) hasta la semana 284
- El estudio excluyó a pacientes con DepCreat ≤10 ml/min.5
Incidencia de ADNemia por CMV cuantificable hasta la semana 28 por cuartil de DepCreat 4,e
- La ADNemia por CMV cuantificable se dividió en cuartiles; Cuartiles: 1 (0 a ≤52 ml/min), 2 (>52 a ≤67 ml/min), 3 (>67 a ≤85 ml/min) y 4 (>85 ml/min).4
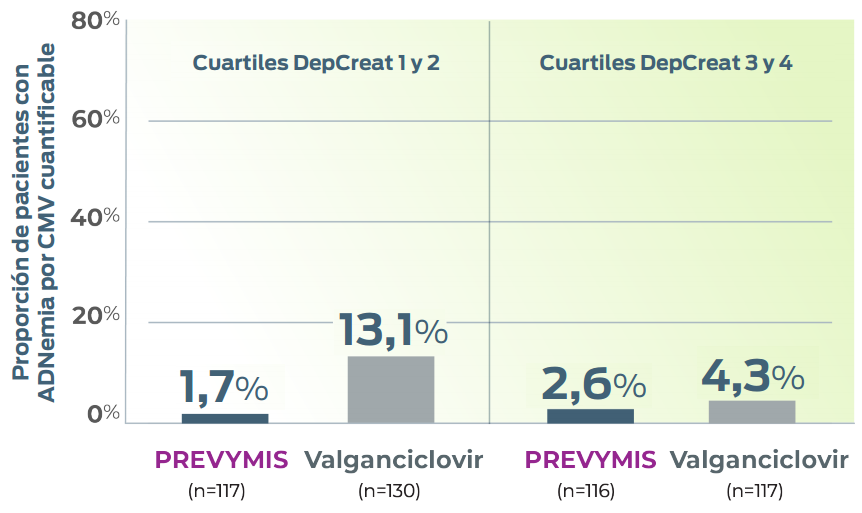
eNo se incluyeron los participantes sin DepCreat en la semana 28.4
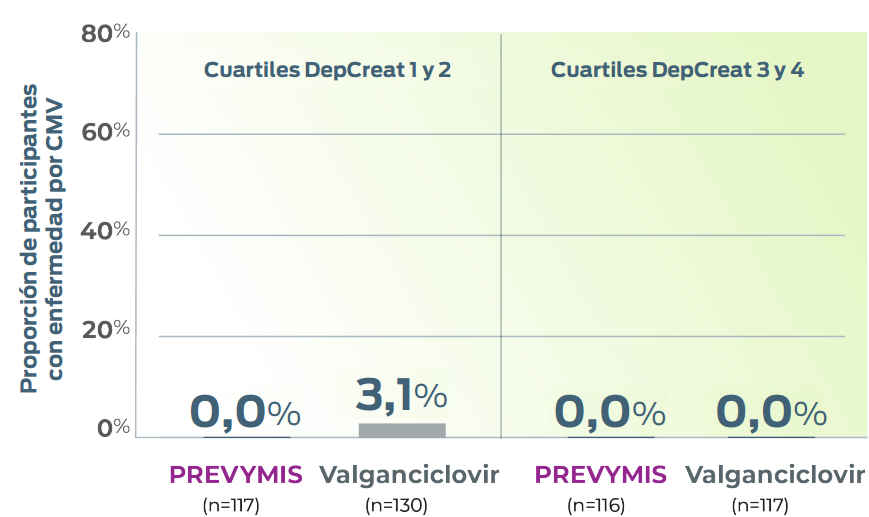
Incidencia de enfermedad por CMV (confirmada mediante adjudicación) hasta la semana 28 por cuartil de DepCreat4,e
- La enfermedad por CMV cuantificable se dividió en cuartiles; Cuartiles: 1 (0 a ≤52 ml/min), 2 (>52 a ≤67 ml/min), 3 (>67 a ≤85 ml/min) y 4 (>85 ml/min).4
Considere la profilaxis contra CMV con PREVYMIS en sus receptores adultos de trasplante de riñón D+/R-2
IC: intervalo de confianza; CMV, citomegalovirus; DepCreat: depuración de creatinina; D+/R-, donante CMV seropositivo/receptor CMV seronegativo; ADN, ácido desoxirribonucleico; OF, fallo observado.
Referencias:
1. Roberts MB, Fishman JA. Immunosuppressive agents and infectious risk in transplantation: managing the “net stateof immunosuppression.” Clin Infect Dis. 2021;73(7):e1302-e1317. doi:10.1093/cid/ciaa1189. 2. Razonable RR, Humar A. Cytomegalovirus in solid organ transplant recipients—Guidelines of the American Society of Transplantation Infectious Diseases Community of Practice. Clin Transplant. 2019:33(9):13512. doi:10.1111/ctr.13512. 3. Limaye AP, Budde K, Humar A, et al. Letermovir vs valganciclovir for prophylaxis of cytomegalovirus in high-risk kidney transplant recipients: a randomized clinical trial. JAMA. 2023;330(1):33-42. doi:10.1001/jama.2023.9106. 4. Budde K, Kamar N, Crespo M, et al. Letermovir vs valganciclovir prophylaxis and risk of cytomegalovirus DNAemia in a randomized phase 3 trial. Poster presented at: European Society for Organ Transplantation (ESOT) Congress: September 17-20, 2023. 5. Limaye AP, Budde K, Humar A, et al. Letermovir vs valganciclovir for prophylaxis of cytomegalovirus in high-risk kidney transplant recipients: a randomized clinical trial. JAMA. 2023;330(1):33-42. Supplement 2:1-13. doi:10.1001/jama.2023.9106. 6. Prevymis Información para prescribir. República Dominicana.
